CGMP
CGMP란?
CGMP는 Cosmetic Good Manufaturing Practice(우수 화장품 제조 및 품질관리기준)의 약어로 품질이 보장된 우수한 화장품을 제조, 공급하기 위해 제조소의 구조, 설비를 비롯, 화장품의 원료, 자재 등의 구입에서부터 제조, 포장 등 모든 공정관리와 출하에 이르는 제조 및 품질관리 전반에 걸쳐 지켜야 할 사항을 규정한 우수 화장품 제조 및 품질관리 기준 준수를 인증하는 식약처기준 입니다.
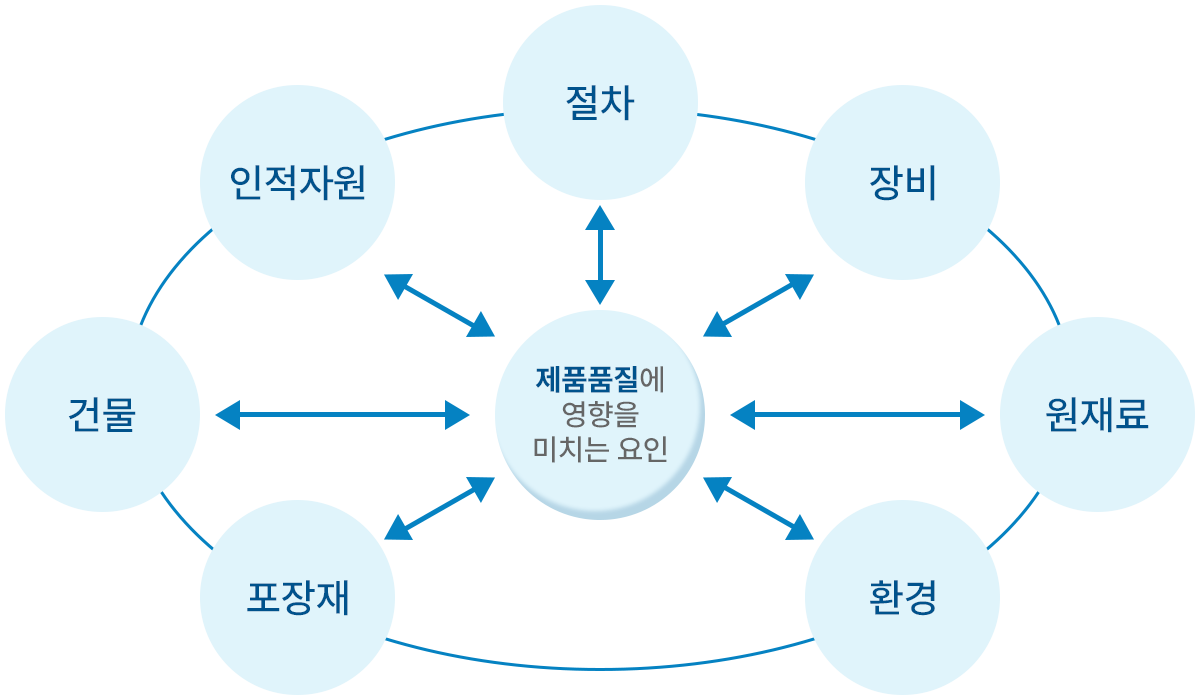
CGMP 구성요소
hard ware
품질이 보장된 우수한 화장품을 제조, 공급하기 위한 제조공장의 구조, 설비(장비) 기준
soft ware
원료, 자재의 구입으로부터 제조, 포장 등 모든 공정관리 제조환경을 청결하게 하여
안전한 화장품을 생산하기 위한 시설, 제품안전 및 공정에 관한 기준
CGMP인증의 기대효과
1
브랜드의 품질경쟁력과 신뢰도 향상
2
정부기관의 강제 의무화 사전 대비
3
생산제품의 법적요건, 제조 및 품질기준 부합성을 보증
4
배치 균일성과 오염 및 규격 이탈의 위험성 감소
5
최종 화장품 제조자의 인증요구에 대비
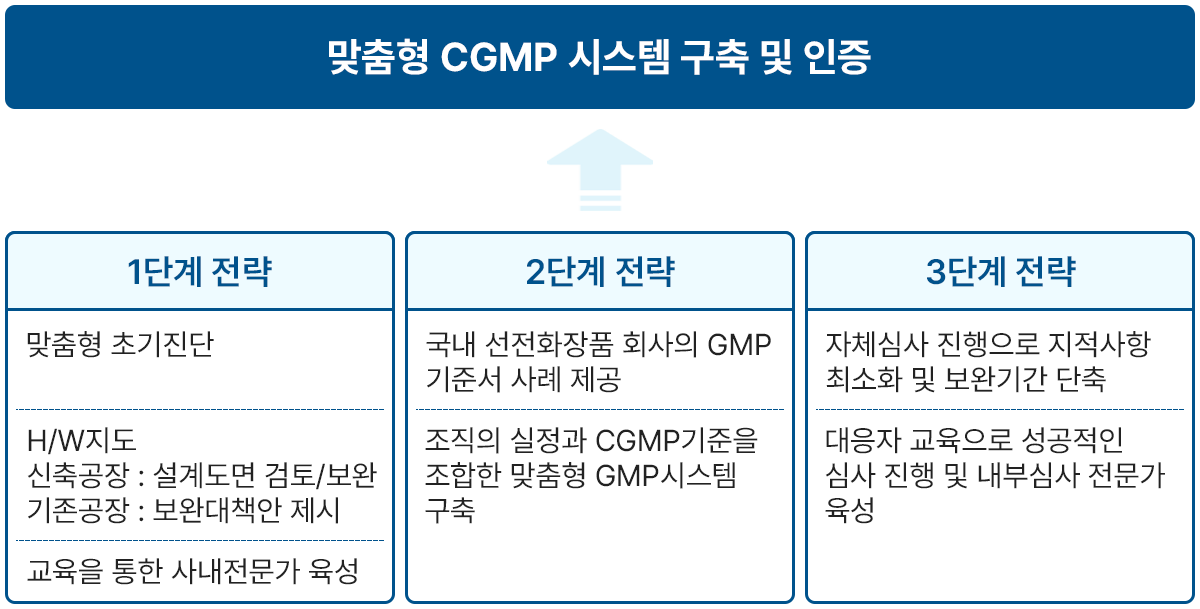
CGMP 컨설팅 추진전략

CGMP 주요 추진항목 및 예상일정
| 단계 | 주요 추진항목 | 세부추진 내용 |
|---|---|---|
| 컨설팅 사전준비 | 컨설팅 안내 | 컨설팅 전반내용 설명(기간/비용/지도방법 등) |
| 고객 요구사항 파악/협의 | 고객의 요구내용/수준, 방향, 일정, 비용 등등 | |
| 회사현황 파악 및 초기 진단 | 현장투어/관련규정/조직도/제품현황/품질관리팀장 인터뷰 등 확인 | |
| 갭(Gap) 분석 | 현재 수준진단 자료을 통한 문제점 분석 | |
| 제안서 제출 | 지도일수/일정/진행방향/비용/지불조건 등 | |
| 계약서 체결 | 제안서 제출내용 검토,표준계약서 작성 | |
| 계획 (Plan) | Kick off 미팅/추진조직 구성 | CGMP 추진 TFT구성(총 책임자/ 실무 책임자/ 부서별 담당자 등) |
| 부서별 업무분장 | 할일에 대한 세부업무 분장 | |
| 전체 CGMP추진일정 계획수립 | 전체 추진 목표일정 계획수립 | |
| 부분별 GMP수준 진단 | 각 부서별 세부 진행현황 및 수준파악 | |
| 세부 할일 및 일정계획 수립 | 문제점에 대한 세부할일/주인/일정계획 수립 | |
| 실행(Do) | 교육(부서별, 계층/수준별) | CGMP개요, 4대기준서(제품표준서/제조관리/제조위생/품질관리) |
| 시설/장비 및 기구보완(H/W) | 작업장 레이아웃 보완(인동선, 물동선, 청정도 등) | |
| 제조지원 시스템(용수,공조,압축공기) 보완 | ||
| 필요한 기구 보완(측정기 구입 및 교정 포함) | ||
| GMP시스템 문서화(S/W) | 문서작성 방법 기본교육 | |
| 사내규정 제/개정 | ||
| 사내규정 실행 | ||
| 각종 규정의 기록서 작성 | ||
| 각종 표시사항 부착 | 각종 설비 및 배관(AIR, 용수 등) 표시라벨 부착(고유번호/종류/방향) | |
| 평가(Check) | 3회시범 운영 및 보완 | 약 2~3주 간격으로 실제 GMP를 자율적으로 실행하여 문제점 파악/보완 |
| CGMP신청서 작성/제출 | 3회운영 문제점/보완 결과서와 CGMP평가신청서를 작성/ 제출 | |
| 개선(Action) | 모의실사(자체) | 2~3회진행 진행, 문제항목 지속보완/ 대응자 교육 등 |
| CGMP실사 | 식약처 실사 | 평가신청서 지적사항/ 보완 |
| 본 실사는 2일간, 2명이 현장실사(본청 직원) | ||
| 지적사항 보완/제출 | 지적사항 사전 보완준비, 약 2주이내에 실사결과 문서로 통보됨 | |
| 지적사항 보완결과서를 제출(1개월 이내), 2회 연장가능 | ||
| CGMP승인 | 보완결과서 제출후 2주이내 GMP승인 공문서 발송 | |
| ※ ISO22716과 동시 추진시는 ISO는 별도의 추가 준비없이 인증심사를 받을수 있음 | ||
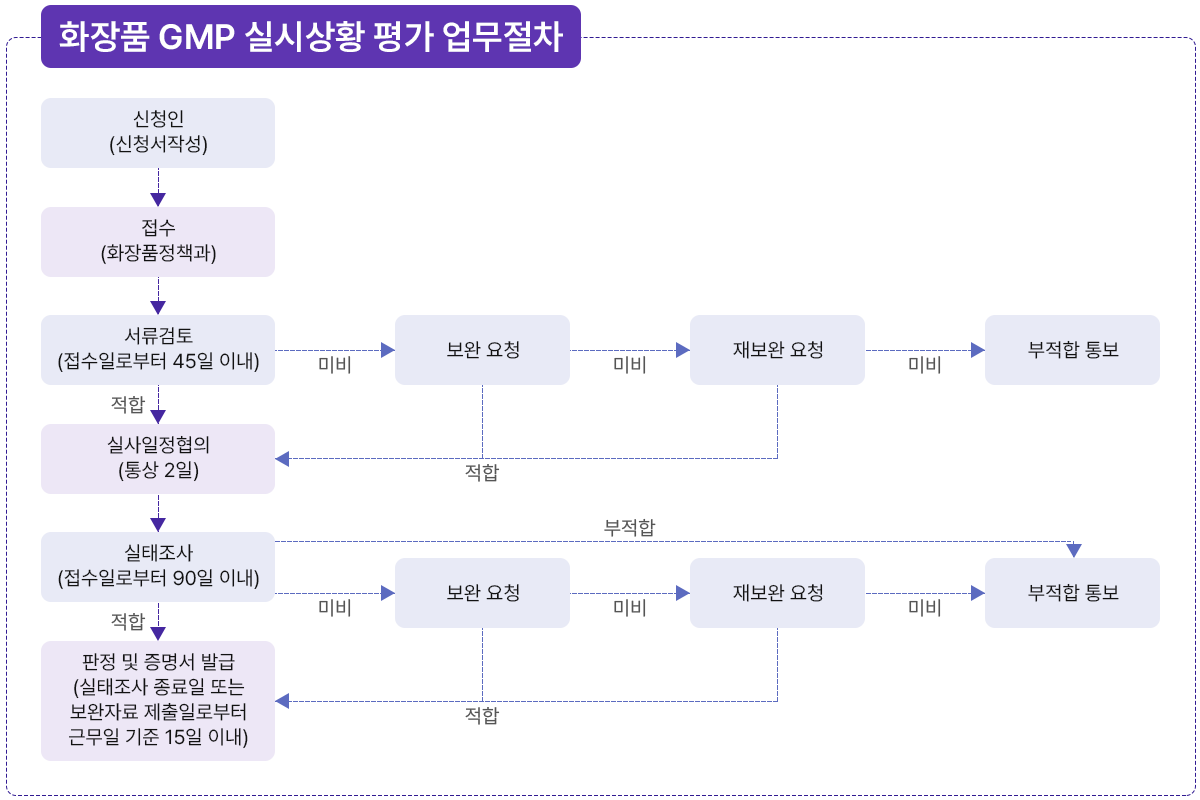
식약처 CGMP실시상황 평가업무 절차